❶Главная
/
❷Медицинские публикации
/
❸Медицинские...
/
❹Тест-системы,...
/
ПСА заг. - IФА
Інструкція
по використанню тест-системи імуноферментної
для визначення загального простата-спецефічного антигена
в сиворотці та плазмі крові
(ПСА заг. - IФА)
Державний реєстраційний номер № 1247/2002
Тільки для досліджувань in vitro.
Набір вироблений по технології та з компонентів фірми Хема-Медіка, Москва.
Введення
Загальний простата-специфiчний антиген (ПСАз) являє собою глікопротеїд з молекулярною масою 34 кДа, що складається з одного поліпептидного ланцюга. ПСА, виробляється епітеліальними клітинами здорової простати та функціонує як серинова протеаза для зменшення в’язкостi сперми.
При гіперплазiї і злоякіснiй трансформацiї простати збiльшується виробка та секрецiя ПСАз в крові.
Зміст ПСАз в сироватцi кровi збільшується з віком, особливо у чоловіків пiсля 40 років.
Показаннями до визначення ПСАз: проведення масового скрининга в чоловiкiв старшого вiку, діагностика та мониторинг лiкування раку предстатевої залози.
Принцип визначення
У наданiй тест-системi використовується принцип двосайтового (сендвiч) iмуноферментного аналiзу. У лунки мiкропланшета, на поверхнi якого адсорбованi специфiчнi анти-ПСАз-антитiла, вносять дослiджуваний зразок. Антиген iз зразка зв'язується з антитiлами на поверхнi лунки. Незв'язаний матерiал видаляється вiдмивкою. У лунку вносять другi антитiла проти iншого епiтопу ПСАз , мiченi пероксидазою. Активнiсть ферменту, зв'язаного на поверхнi лунки мiкропланшету, проявляється i вимiрюється додаванням хромоген-субстратної сумiшi, стоп-розчину та фотометрiєю при 450 нм. Iнтенсивнiсть кольорової реакцiї прямо пропорцiйна кiлькостi специфiчних антитiл у зразку.
Склад набору :
- Анти-ПСАз IФА стрипи, 8х12 лунок ( 1 шт.)
- Стрічка для закліювання стрипів ( 1 шт.)
- IФА буфер синiй, 11 мл ( 1фл.)
- Набiр калiбраторiв та контролiв, по 0.6 мл (всього 5 калiбраторiв: 0; 1.5; 5; 10, 30 нг/мл; та 1 контрольний зразок)
- Концентрат вiдмиваючого розчина, 22 мл (1 фл.)
- Кон'югат, 11 мл ( 1 фл.)
- Субстрат , 11 мл ( 1 фл.)
- Стоп-розчин, 11 мл (1 фл.)
Важливі зауваження по збереженню реагентів і виконанню тесту.
1. Не змішуйте і не використовуйте в одній постановці реагенти різних серій.
2. Після використання реагенту негайно закривайте кришку флакона чи пробірки. Увага: закривайте кожен флакон своєю кришкою.
3. Усі компоненти набору повинні зберігатися в холодильнику (+2…+100С ). Не заморожуйте набір.
4. Після розкриття пакета ретельно заклейте лунки, що залишилися, стрічкою для закліювання, яка входить до складу набору, щоб запобігти впливу вологи пiд час зберiгання.
5. Увага! Під час всіх інкубацій необхідно заклеювати планшет клейкою стрічкою. Не допускайте пересихання лунок мікропланшета між стадіями постановки.
6. Усі проби і стандарти бажано ставити в двох паралелях (повторах).
7. Досліджувані сироватки повинні бути ретельно отцентрифуговані. Не використовуйте мутні, хильозні та гемолітичні зразки.
8. Якщо аналіз виробляється не в день узяття крові, сироватку варто зберігати при -200С. Повторне заморожування-відтавання не допускається.
9.Відмивання мікропланшета може проводитися як вручну, так і з використанням автоматичних пристроїв. Вносите не менш 200 мкл відмивочного буфера у лунки при кожному відмиванні. Затримка при відмиванні («замочування») не потрібна. Після закінчення ручного відмивання різко перегорнiть мікропланшет на фільтрувальний папір для видалення залишків буфера.
10. Вимірюйте оптичну щільність протягом не більш 15 хвилин після зупинки реакції із субстратом.
Підготовка реагентів
1. Усі реагенти (включаючи необхідне число стрипів) перед використанням повинні бути доведені до кімнатної температури (20-25°С).
2. Приготуйте Відмиваючий розчин: для цього концентрат розбавте 10-кратним об’ємом дистильованої води в чистому посуді.
Проведення визначення
1.
Помістiть у рамку потрібну кількість стрипів - зразки в 2 повторах та 12 лунок для калiбраторiв та контрольних зразкiв.
2. Внесiть у лунки по 50 мкл Синього IФА буфера.
3. Внесiть у лунки по 50 мкл калiбратора або дослiджуваного зразка.
4. Iнкубуйте 30 хвилин при температурi 37С.
5. Вiдмийте стрипи 3 рази видмивочним розчином.
6. Внесiть у лунки по 100 мкл розчина кон'югата.
7. Iнкубуйте 30 хвилин при температурi 37°C.
8. Вiдмийте стрипи 5 разiв вiдмиваючим розчином.
9. Внесiть у лунки 100 мкл субстратного розчина.
10. Iнкубуйте 15 хвилин при температурi 20-25° C.
11. Внесiть у лунки 100 мкл стоп-розчина.
12. Визначте оптичну щільність у лунках на фотометрі при довжині хвилі 450 нм .Бланк фотометра виставляйте проти нульового калібратора.
Примітка : Інкубацію при температурі 37°С можно заменити інкубацією при 20-25С при постійному струшуванні.
Приклад калібровочної кривої ( ось Х – конц.; ось У – ОЩ нг/мл )
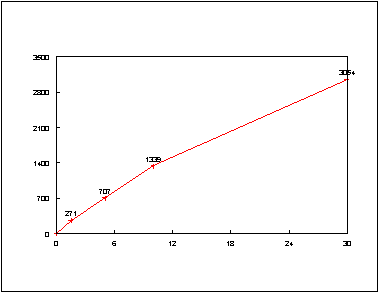
Очікувані коливання контрольного зразка 6 – 12 нг/мл.
Нормальні величини:
Грунтуючись на результатах досліджень, проведених лабораторiями, рекомендуємо скористатися нормами, приведеними нижче. Разом з тим, відповідно до правил GLP (Гарної лабораторної практики), кожна лабораторія повинна сама визначити для себе параметри норми, характерні для обстежуваної популяції.
Чоловіки : до 40 років --- верхня межа-4,0 нг/мл.;
41 – 60 років --- верхня межа –7,0 нг/мл.
більш 61 рік --- верхня межа –10,0 нг/мл.
Жінки : --- верхня межа –0,45 нг/мл.
Вимоги безпеки
1. Набір призначений тільки для діагностики in vitro. Категорично забороняється піпетування ротом.
2. Засобами індивідуального захисту при роботі з наборами є марлеві пов’язки та гумові рукавички.
3. Знезараження сироваток проводити згiдно з наказом МОЗ СРСР №408 вiд 29.12.89 р. «О мерах по снижению заболеваемости вирусными гепатитами в стране».
Умови транспортування
1. Набори транспортують всіма видами закритого транспорту при температурі від +4 до +100С. Допускається транспортування при температурі до + 370С не більше 72 годин.
2. Набори повинні зберігатися при температурі від +4 до +100С. Не допускається замороження!
Гарантії виробника
1. Виробник гарантує відповідність якості наборів вимогам цих ТУ при додержанні споживачем наведених у них умов транспортування та зберігання.
2. Гарантійний термін зберігання становить 6 місяців від дня виготовлення набору. Після закінчення терміну зберігання набори підлягають переконтролю з метою перевірки їх працездатності
3. Термін придатності стрипів після розкриття пакету становлює 1 місяць при температурі +2...+10˚ С. Невикористані стрипи зберігають у щільно закритому пакеті!
|


